- ST
Soolestiku kolonisatsioon esimesel 1000 elupäeval ja kasu tervisele
Tuhat elupäeva on konkreetne ajavahemik inimese elueas, mis algab rasestumisest ja kestab läbi imikuea ja lapsepõlve. Kuigi periood on võrreldes kogu eluperioodiga suhteliselt lühike, mõjutab see suurel määral inimese edasist tervist ja heaolu kogu järgneva elu jooksul, sest just sel perioodil toimub soolestiku koloniseerimine erinevat tüüpi mikrobiootaga.
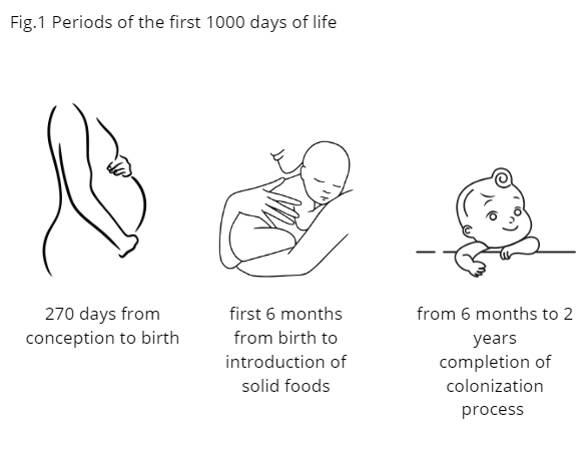
Esimese 1000 päeva eluperioodi võib jagada kolmeks erinevaks osaks (joonis 1):
I. sünnieelne osa kestab rasestumisest kuni sünnituseni ja vältab keskmiselt 270 päeva. Ema tervis ja mikrobioota on loote tervise ning edasise arengu seisukohast väga olulise tähtsusega;
II. esimesed 6 elukuud või 270.-450. päev kestab sünnist kuni tahke toidu kasutuselevõtmiseni ja seda iseloomustab ainult või valdavalt piimaga toitmine (rinnapiim, piimasegu või nende kombinatsioon);
III. ajavahemik 6. elukuust kuni 2. eluaastani või 450.-1000. päev lõppeb 2aastaselt, kui kolonisatsiooniprotsess jõuab lõpule ja moodustub täiskasvanu tüüpi mikrobioota.
Mikrobioota kolonisatsioon esimesel 1000 elupäeval
Esimese 1000 elupäeva jooksul määravad mikrobioota kolonisatsiooni mitmesugused tegurid.
Esimesel ehk sünnieelsel perioodil määravad vaginaalse kolonisatsiooni ema tervis, toitumine ja antibiootikumide kasutamine. Mitu aastat arutleti selle üle, kas loote kolonisatsioon toimub ka raseduse ajal, kuid viimasel ajal on jõutud üksmeelele, et see algab sündimisel ja vaginaalne sünnitus on kolonisatsiooniprotsessis väga oluline.
Lactobacillus'e liigid, mis tavaliselt domineerivad terves tupe mikrobioomis, aitavad positiivselt kaasa tulevase lapse soolestiku tervisele. Tegurid, mis häirivad vaginaalset kolonisatsiooni, võivad kahjustada lapse tervisliku mikrobioota arengut tulevikus.
Teisel perioodil enne tahke toidu kasutuselevõtmist määravad lapse mikrobiootat peamiselt sellised tegurid nagu sünnituse tüüp (vaginaalne või keisrilõige) ja toitmise tüüp (ainuüksi rinnaga toitmine, piimasegu või segatoitmine). Domineerivad Bifidobakterid ja Lactobacillus, mis soodustavad rinnapiima seedimist ja immuunsüsteemi arengut. Muud tegurid, mis võivad mõjutada mikrobiootat teisel perioodil, on sünnikaal, infektsioonid, hügieen ja muud tegurid .
Kolonisatsiooniprotsess kolmandal perioodil pärast tahkete toitude kasutuselevõtmist on keerulisem ja seda määravad mitmed tegurite rühmad, nagu toitumine, rinnaga toitmise jätkumine, antibiootikumide kasutamine ja muud tegurid, nagu kokkupuude keskkonnaga, hügieeni harjumused ja isegi unemustrid. Imikute soolestiku mikrobioota mitmekesistub kiiresti ja see mitmekesistumine loob eeldused tulevase tervise jaoks ning mõjutab selliseid aspekte nagu immuunsus, toitainete imendumine ja vastuvõtlikkus haigustele.
Soolestiku immuunsüsteemi areng paralleelselt mikrobioota kujunemisega
Esimese 1000 päeva jooksul on immuunsüsteemi rakkude arv soolestikus peaaegu olematu, kuid soolestikuga seotud lümfikoed hakkavad ema mikrobioota toimel kiiresti arenema. Esialgu domineerivad Bifidobakterid ja Lactobacillus, need nn sõbralikud bakterid aitavad rinnapiima seedida ja õpetavad immuunsüsteemi eristama kahjutuid ja kahjulikke mikroobe.
Rinnapiimal on oluline roll varajase mikrobioota kujundamisel selliste komponentide kaudu nagu sekretoorne immunoglobuliin A (SIgA), mis aitab soodustada kasulike bakterite kasvu.
Antigeenide imendumine soolest on piimaga toitmise perioodil piiratud ning see on tingitud kahest tegurist:
• karikrakkudeseoseliste koridoride (GAP) puudumine: need on spetsiifilised struktuurid soole limaskestas, mis võimaldavad antigeenidel immuunsüsteemi järelevalvest mööda minna. Vastsündinutel ei ole GAP-d täielikult välja arenenud.
• ebaküpsed M- rakud: need rakud transpordivad tavaliselt antigeene soolestikuga seotud lümfikoe (GALT) immuunsüsteemi rakkudesse. Vastsündinutel ei funktsioneeri need veel täiel määral.
Piiratud kokkupuute tõttu antigeenidega jäävad soolestikus olevad lümfotsüüdid (T- ja B-rakud) kogu varase postnataalse perioodi jooksul suures osas naiivseteks, mis tähendab, et nad ei ole kokku puutunud spetsiifiliste antigeenidega ning välja ei ole kujunenud immuunvastust.
Pärast rinnast võõrutamist väheneb rinnapiima ja selle kaitsva sekretoorse immunoglobuliini A (SIgA) sisaldus soolestiku luumenis. See vähendab esialgset kaitset võimalike patogeenide ja mikroobide antigeenide vastu ning alguse saavad järgmised protsessid: suurenenud kokkupuude antigeenidega, mikroobide stimuleerimine, millele järgneb immuunvastus ja idukeskuste moodustumine.
Suurenenud kokkupuudet antigeenidega, mikroobide stimuleerimist immuunvastusega ja idukeskuste moodustamist võib iseloomustada kui immuunsüsteemi käivitamist: koordineeritud sündmuste jada on võõrutusreaktsioon. See ei ole täiemahuline immuunrünnak, vaid pigem kontrollitud aktiveerimine, mille eesmärk on algatada kohandatud immuunvastus ja vältida ülestimuleerimist.
Lisaks sellele korraldavad soolestikuga seotud lümfoidkoe küpsemist kaks paralleelset protsessi: immuunsüsteemi väljaõpetamine ja vastastikune kujundamine.
Immuunsüsteemi õpetamise protsessis toimivad mikroobid antigeenidena, õpetades immuunsüsteemi rakke ära tundma ja taluma kahjutuid mikroobe, olles samal ajal valmis reageerima patogeenidele. See õrn tasakaal on ülioluline, et vältida ebavajalikke immuunreaktsioone, nagu allergiad ja autoimmuunhaigused.
Vastastikuse kujundamise käigus reguleerivad antibakteriaalsed molekulid ja immuunsüsteemi rakud bakterite populatsioone, samas kui spetsiifilised bakterite metaboliidid võivad moduleerida immuunvastuseid. See pidev dialoog aitab kaasa terve soolestiku ökosüsteemi ja üldise immuunsüsteemi toimimise säilitamisele.
Soolestiku kolonisatsiooni epigeneetiline mõju esimese 1000 elupäeva jooksul mittenakkuslike haiguste arengule
Soolestiku kolonisatsioon esimesel 1000 elupäeval mõjutab mittenakkuslike haiguste, nagu südame-veresoonkonna haigused, diabeet, kroonilised hingamisteede haigused ja vähk, arengut (Joonis 2).
Mikrobioota mõju mittenakkuslike haiguste arengule avaldub epigeneetiliste mehhanismide kaudu. Epigeneetiline mehhanism määrab geeniekspressiooni DNA järjestust muutmata. Esimesed 1000 päeva on eluperiood, mil epigeneetilise DNA-süntees on kõige aktiivsem. Selles varajases arenguetapis võivad toitumine ja mikrobioomi koostis mõjutada geenide ekspressiooni, mis võib suurendada või vähendada tõenäosust, et hilisemas elus tekivad sellised kroonilised haigused nagu südame-veresoonkonna haigused, rasvumine ja diabeet.
Sünnieelne ja sünnieelne ennetav sekkumine
Kaks peamist tegurit, mis soodustavad imikute tervislikku soolestiku koloniseerimist, on ema tervis ja sünnituse viis.
Ema tervise toetamine
1. Ema mikrobioota mõjutamine raseduse ajal (funktsionaalne toit, probiootikumid ja prebiootikumid). Spetsiifiliste prebiootikumide või probiootikumide tarbimine raseduse ajal võib soodustada kasulike bakterite teket emal, mõjutades tõenäoliselt lapse esmast soolestiku kolonisatsiooni. Käimasolevate uuringute käigus uuritakse konkreetseid tüvesid, annuseid ja kasu erinevatele rasedusetappidele.
2. Ema parodondihaiguste ravi. Ravimata parodondihaigus on seotud kahjulike bakterite vohamisega, mida võib seostada enneaegse sünnituse ja madala sünnikaaluga, mis tõenäoliselt mõjutab lapse esmast kokkupuudet mikrobioomiga. Selle haiguse ravi võib vähendada kahjulike bakterite ülekandumist ja soodustada lapse tervislikumat soolestiku keskkonda.
3. Infektsioonide ravi. Teatud rasedusaegsed infektsioonid võivad negatiivselt mõjutada ema ja lapse mikrobiootat. Tõhus infektsioonivastane strateegia, nagu vaktsineerimine, hügieeniharjumused ja kõrge riski minimeerimine, võivad kaitsta mõlemaid ja luua tervema soolestiku keskkonna lapsele.
4. Toitumise parandamine (üle- või alatoitumine). Nii ema ala- kui ka ületoitumine võivad mõjutada lapse arenevat mikrobiootat. Tasakaalustatud ja piisava toitumise tagamine raseduse ajal soodustab lapse tervislikumat mikroobikolonisatsiooni.
Vaginaalse sünnituse eelistamine, kui see on ohutu ja võimalik, ning riskide vähendamine keisrilõike korral
Sünnituse ajal puutub sünnituskanalit läbiv laps kokku ema tupe mikrobiootaga, omandades erinevaid baktereid. See esialgne kolonisatsioon loob aluse lapse enda soolestiku mikrobioota kujunemisele. Keisrilõike teel sündinud lastel selline kokkupuude puudub, mille tulemusena on nende esmane mikrobioomi koostis erinev. Neil on sageli vähem Bifidobaktereid ja Lactobacillust, rohkem oportunistlikke haigustekitajaid, nagu Clostridium difficile ja Streptococcus. Vaginaalse sünnituse ja keisrilõike teel sündinud laste mikrobiootade erinevused võivad püsida kuni väikelapseeani.
Uuringud näitavad, et need varajased erinevused võivad soodustada keisrilõike teel sündinud lastel teatud terviseprobleemide teket, sealhulgas allergiate ja astma , autoimmuunhaiguste , rasvumise ja põletikulise soolehaiguse suurenenud riski. Tõendid on siiski komplekssed. Praegu käivad uuringud, et selgitada välja soolestiku mikrobioota koostise, geneetilise eelsoodumuse, rinnaga toitmise tavade ja toitumisega seotud rolli sünnitamisviisi mõju vahendamisel. Lisaks uuritakse probiootikumide manustamise ja vaginaalse bakteriaalse külvamise võimalikku kasu. Hiljuti läbi viidud uuringus, mille käigus teostati vaginaalne mikroobide külvamine, ei õnnestunud tõestada soolestiku mikrobioota struktuuri ja funktsiooni paranemist ning bakteroidide taseme taastumist imikutel, kes sündisid plaanilise keisrilõikega.
Andmed probiootikumide kohta on paljulubavamad. Nii näitas uuring, milles uuriti probiootilist tüve Lactobacillus reuteri DSM 17938 sisaldava piimasegu mõju keisrilõikega sündinud imikute väljaheite mikrobiootale, et alates 2 nädala vanusest muutus väljaheite mikrobioota üldine koostis oluliselt sarnasemaks vaginaalselt sündinud imikute mikrobiootaga. Imikute rühmas, kes said piimasegu koos probiootilise tüvega Lactobacillus reuteri DSM 17938, oli Bifidobacterium, Collinsella ja Lactobacillus arvukus suurem võrreldes imikutega, kes said kontrollpiimasegu. Keisrilõikega sündinud imikute puhul muutis see konkreetse probiootilise koostisega preparaat väljaheite mikrobioota varajast arengut nii, et selle koostis oli sarnasem vaginaalselt sündinud imikute mikrobiootaga .
Sünnitusjärgne sekkumine
Sünnitusjärgne sekkumine sobilikuma kolonisatsiooni toetamiseks põhineb toitumisel, prebiootikumide ja probiootikumide kasutamisel ning antibiootikumide kasutamise minimeerimisel.
Rinnapiim ei paku imikutele mitte ainult täielikku personaalset toitu, omades seejuures olulist tähtsust optimaalse kasvu ja arengu jaoks, vaid tagab ka immunoloogilise kaitse kriitilisteks eluperioodideks. Imetamise kaudu kantakse emalt imikule üle stimuleerivate, arengut soodustavate signaalide ja põletikuvastaste ühendite kogum. Kõige tugevamad immunoreguleerivad faktorid on tsütokiinid, kasvufaktorid, spetsiifilised valgud, nagu laktoferriin, peptiidid, rasvhapped, inimpiima oligosahhariidid ja mikroobid . Ajalooliselt peeti rinnapiima steriilseks vedelikuks, kuid see arusaam on viimastel aastatel muutunud. Bakterikultuurist sõltuvad meetodid näitasid mikroobide olemasolu piimas, peamiselt stafülokokkide, streptokokkide, laktobatsillide ja Bifidobacterium spp. olemasolu. Hiljuti arendatud bakterikultuurist sõltumatud meetodid kinnitasid mikrobiaalse DNA olemasolu ning mikroobide rikkaliku ja mitmekesise kogukonna olemasolu rinnapiimas. Hinnanguliselt sisaldab 1 ml rinnapiima 104 -107 CFUd baktereid. Rinnapiima saavate imikute soolestiku mikrobioota on mitmekesisem ja stabiilsem kui rinnapiimaasendajat saanud imikutel ning sellel on märkimisväärne positiivne mõju immuunsüsteemi arengule.
Funktsionaalsed toitained, mis moduleerivad soolestiku mikrobiootat
Kui rinnaga toitmine ei ole mingil põhjusel võimalik, võib mikrobioota puudujäägi korvamiseks kasutada mitmesuguseid probiootikume, prebiootikume, sünbiootikume ja postbiootikume.
Prebiootikumid (substraat, mida peremees-mikroorganismid valikuliselt kasutavad, andes kasu tervisele) võivad asendada rinnapiima toitvaid kiudaineid, soodustades potentsiaalselt kasulike soolebakterite teket ja tootes lühikese ahelaga rasvhappeid (SCFA), mis omakorda soodustavad regulatiivsete T-rakkude arengut, pärsivad põletikuvastust ja optimeerivad oluliste toitainete, nagu vitamiinide ja mineraalide, imendumist.
Probiootikumid (elusad mikroorganismid, mis piisavas koguses manustatuna avaldavad kasulikku toimet peremeesorganismile). Probiootikumid esindavad spetsiifilisi elusaid mikroorganisme, mis võistlevad potentsiaalselt kahjulike patogeenidega, takistades nende levikut ja soodustades kasulike bakterite kasvu.
Sünbiootikumid on määratletud kui toidulisandid või toiduained, milles on kombineeritud probiootikumid ja prebiootikumid. Selle kombinatsiooni eesmärk on kasutada nende kahe komponendi sünergilist mõju, et optimeerida soolestiku tervist ja mõjutada laiemaid tervisetulemusi. Kuigi sünbiootikumide idee kõlab väga hästi, on andmed sünbiootikumide kasutamise kohta pediaatrias piiratud.
Postbiootikumid on elutute mikroorganismide ja/või nende komponentide preparaadid, mis avaldavad kasulikku toimet peremeesorganismile. Postbiootikumid ei sisalda elusaid baktereid. Need on kas terved inaktiveeritud mikroobirakud või nendest rakkudest saadud spetsiifilised komponendid, näiteks metaboliidid. Hiljutised metaanalüüsid näitasid, et postbiootikumide lisamine imiku piimasegule suurendas väljaheite immunoglobuliin A kontsentratsiooni, ilma et see oleks oluliselt mõjutanud imiku koolikute, kõhupuhituse, kõhulahtisuse, oksendamise, kõhuvalu, seedetrakti häirete, päevase kaalutõusu, kehapikkuse kogukasvu ja päevase peapiirkonna suurenemise esinemissagedust. Metaanalüüsi kaasatud uuringud näitasid postbiootikumide ohutust, kuid selle lähenemisviisi tõhususe tõestamiseks on vaja täiendavaid uuringuid.
Antibiootikumide kasutamine
Antibiootikumid, eriti kui neid kasutatakse varases eas, võivad põhjustada püsivaid muutusi mikrobiootas, mis on immuunsüsteemi arengu seisukohalt võtmetähtsusega. Selline sekkumine võib suurendada immuunsüsteemi poolt põhjustatud haiguste riski ja suurendada rasvumise riski hilisemas elus.
Probiootikumide kasutamine koos antibiootikumidega võib tasakaalustada antibiootikumide negatiivset mõju mikrobiootale. Enamik andmeid probiootikumide vastuolulise mõju kohta on seotud antibiootikumidega seotud kõhulahtisuse andmetega. Viimane Cochraini metaanalüüs (2019) probiootikumide kohta antibiootikumidega seotud kõhulahtisuse ennetamiseks lastel näitas AAD (antibiotic-associated diarrhea) vähenemist RR=0,45 (95% CI 0,36-0,56) ja AAD episoodide kestuse lühenemist.
Järeldused
• Soolestiku kolonisatsioon sünnihetkel omab olulist rolli vastsündinu soolestiku immuunsüsteemi ja ainevahetuse arenemisel;
• See areng, eriti esimese 1000 päeva jooksul, on võtmetähtsusega ja määrab imikuea ja hilisema eluperioodi tervise ja haiguste esinemise;
• Peame ennetama või ravima düsbioosi, et tagada õige mikrobioota kolonisatsioon;
• L. Reuteri DSM 17938 lisamine näib ennetavat düsbioosi keisrilõikega sündinud imikutel.
Seotud lood
Tervishoiutöötajatest on Eestis suur nappus, seda eriti suurtest keskustest väljaspool. Saaremaa vald, kohalikud ettevõtjad ning Kuressaare Haigla on leidnud ja rakendanud aga mitut erinevat meedet, kuidas üheskoos seda olukorda parandada ja arste saarele tööle saada.
Enimloetud
5
Viimased uudised
Hetkel kuum
Liitu uudiskirjaga
Telli uudiskiri ning saad oma postkasti päeva olulisemad uudised.
Tagasi Meditsiiniuudised esilehele